Contenu
- Différence principale
- Évaporation vs condensation
- Tableau de comparaison
- Qu'est-ce que l'évaporation?
- Exemple
- Qu'est-ce que la condensation?
- Exemple
- Différences Clés
- Conclusion
Différence principale
La principale différence entre l'évaporation et la condensation est que l'évaporation est le processus de transformation de l'état liquide en état gazeux, tandis que la condensation est le processus de transformation de l'état gazeux en état liquide.
Évaporation vs condensation
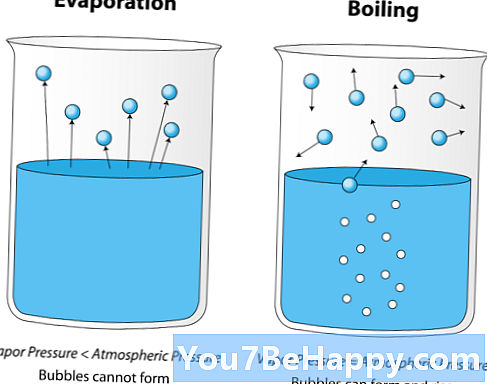
L'évaporation est le processus par lequel une substance passe de la phase liquide à la phase gazeuse, tandis que la condensation est le processus par lequel une substance passe de la phase gazeuse à la phase liquide. L'évaporation se produit à n'importe quelle température juste en dessous du point d'ébullition, mais la condensation se produit à une température constante. L’évaporation se produit lorsque le niveau d’énergie d’une substance augmente et que ses molécules se déplacent plus rapidement et s’échappent de la tension superficielle dans la région environnante; en revanche, la condensation se produit lorsque la température réduite en volume d’air saturé en molécules de la substance provoque la condensation lorsque les molécules perdent leur l'énergie et commencer à combiner jusqu'à ce qu'ils deviennent des gouttelettes de solution. L'évaporation se produit lorsque la pression est basse et la température élevée, au contraire, la condensation se produit lorsque la pression est élevée mais diminue la température. En évaporation, un liquide suffisamment chauffé et les forces d'attraction entre molécules n'empêchent pas leur mouvement de se séparer, puis le liquide s'évapore en gaz, du côté inverse, en condensation, suffisamment refroidi par le gaz, ainsi que les forces d'attraction entre molécules empêchez-les de se déplacer séparément, puis le gaz se condense en liquide ou en solide. L'évaporation peut se produire à tout moment, sur toutes les surfaces et à tous les endroits, alors que la condensation n'a lieu que sur les particules de carbone, les grains de pollen de noyaux hygroscopiques et sur les sels, etc.
Tableau de comparaison
| Évaporation | Condensation |
| L'évaporation est un processus de transformation de la phase liquide en vapeurs / gaz. | La condensation est le processus de transformation des vapeurs / gaz en liquide ou en gouttelettes d’eau. |
| Changement de phase | |
| Changer de liquide en vapeur. | Changer de vapeur en liquide. |
| Affect sur les environs | |
| Il absorbe l'énergie des environs. | Libère de l'énergie dans l'environnement. |
| Point de température | |
| La température en tout point juste en dessous du point d'ébullition. | La température reste constante. |
| Conditions | |
| La température est élevée; la pression est basse. | La pression est forte. la température est basse. |
| Occurrence | |
| Tout le temps, sur toutes les surfaces et à tous les endroits. | Ne se produit que sur les particules de carbone et sur les sels, etc. |
| Force d'attraction | |
| Ne les empêchez pas de se déplacer séparément. | Empêchez-les de se déplacer séparément. |
| Energies cinétiques | |
| Il a une large gamme d'énergies cinétiques. | Il a une petite gamme d'énergies cinétiques. |
Qu'est-ce que l'évaporation?
L'évaporation est le processus par lequel une substance passe de sa phase liquide à sa phase gazeuse. L'évaporation se produit lorsque la pression est basse et que la température est élevée. En évaporation, un liquide chauffe suffisamment et les forces d’attraction entre les molécules ne les empêchent pas de se déplacer séparément; alors le liquide s'évapore sous forme de gaz. L'évaporation se produit à n'importe quelle température juste en dessous du point d'ébullition. L'évaporation se produit lorsque le niveau d'énergie d'une substance augmente et que ses molécules se déplacent plus rapidement et échappent de la tension superficielle à l'environnement. En évaporation, ils absorbent l'énergie des environnements. L'énergie cinétique des molécules liquides est élevée et certaines ont assez d'énergie pour vaincre les forces attractives qui les maintiennent liées. En utilisant cette énergie, les molécules deviennent excitées et atteignent un niveau de saturation maximal qui les convertit en forme gazeuse. . L'évaporation joue un rôle important dans le cycle de l'eau dans lequel les molécules sont entraînées par le vent, puis se condensent finalement sous forme de nuages, ce qui provoque des pluies. L'évaporation se produit à basse altitude tout le temps, sur toutes les surfaces et à tous les endroits.
Exemple
La sueur sur la surface externe d'un verre froid s'évapore lorsque le verre devient chaud.
Qu'est-ce que la condensation?
La condensation est la méthode par laquelle une substance passe de sa phase gazeuse à une phase liquide ou à de minuscules gouttelettes d’eau. La condensation se produit lorsque la température réduite dans le volume d'air saturé en molécules de substance provoque une condensation, car les molécules perdent leur énergie et commencent à se combiner jusqu'à devenir des gouttelettes de solution. La condensation se produit lorsque la pression est élevée, mais la température a diminué. Des réactions exothermiques se produisent lors de la condensation et de l'énergie libérée dans l'environnement, provoquant une augmentation de la température. En outre, la condensation est le changement de phase quelle que soit la température. La condensation se produit principalement à des altitudes plus élevées et des particules de carbone, des grains de pollen de noyaux hygroscopiques et sur des sels, etc.La condensation joue également un rôle dans le cycle de l'eau dans lequel les molécules sont entraînées par le vent; puis ils se condensent finalement sous forme de nuages provoquant des pluies.
Exemple
La vapeur d'eau se condense et forme de la sueur à l'extérieur du verre ou de la canette.
Différences Clés
- L'évaporation est le processus de transformation de l'état liquide en état gazeux, tandis que la condensation est le processus de transformation de l'état gazeux en état liquide.
- L'évaporation se produit à n'importe quelle température juste en dessous du point d'ébullition, mais la condensation se produit à une température constante.
- L’évaporation se produit lorsque le niveau d’énergie d’une substance augmente et que ses molécules se déplacent plus rapidement et s’échappent de la tension superficielle dans la région environnante; en revanche, la condensation se produit lorsque la température réduite en volume d’air saturé en molécules de la substance provoque la condensation lorsque les molécules perdent leur l'énergie et commencer à combiner jusqu'à ce qu'ils deviennent des gouttelettes de solution.
- L'évaporation se produit lorsque la pression est basse et la température élevée, au contraire, la condensation se produit lorsque la pression est élevée mais diminue la température.
- L'évaporation absorbe l'énergie du milieu environnant, tandis que la condensation libère de l'énergie vers le milieu environnant.
- L'évaporation peut se produire à tout moment, sur toutes les surfaces et à tous les endroits, alors que la condensation n'a lieu que sur les particules de carbone, les grains de pollen de noyaux hygroscopiques et sur les sels, etc.
Conclusion
La discussion ci-dessus conclut que l'évaporation est le processus de transformation de l'état liquide en état gazeux, alors que la condensation est le processus de transformation de l'état gazeux en état liquide.